Citidinas priklauso nukleozidams ir yra sudarytas iš nukleozinės bazės citozino ir cukraus ribozės. Per vandenilio ryšį jis sudaro bazinę porą su guanozinu. Jis taip pat vaidina pagrindinį vaidmenį pirimidino metabolizme.
Kas yra citidinas?
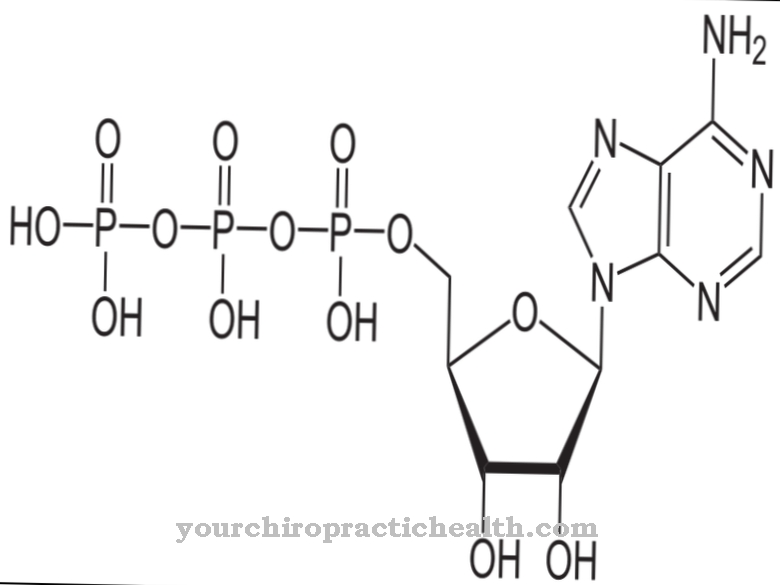
Citidinas yra nukleozidas, kurį sudaro citozinas ir ribozė. Be adenino, guanino ir timino, azoto bazės citozinas dalyvauja nukleorūgščių sintezėje. Fosforilinant citidiną, susidaro citidino monofosfatas (CMP), citidino difosfatas (CDP) arba citidino trifosfatas (CTP).
Citidinmonofosfatas yra RNR nukleotidas. Nukleorūgščių struktūroje dalyvauja dvi purino ir dvi pirimidino bazės. RNR timinas keičiamas uracilu. Adeninas ir guaninas priklauso purino bazėms, o timinas, citozinas ir uracilas priklauso pirimidino bazėms. Citidindeaminazė gali dezaminuoti citidiną į uridiną. Uridinas yra nukleozidas, pagamintas iš ribozės ir uracilo. Jis taip pat gali būti fosforilintas iki uridino monofosfato.
Uridino monofosfatas taip pat yra svarbus RNR nukleotidas. Be to, CDP ir CTP taip pat yra aktyvinančios grupės lecitino, cefalino ir kardiolipino sintezei. Grynas citidinas yra vandenyje tirpi kieta medžiaga, kuri skyla esant 201–220 laipsnių temperatūrai. Fermentas pirimidino nukleozidazė jį kataliziškai gali skaidyti į citoziną ir ribozę.
Funkcija, poveikis ir užduotys
Citidinas vaidina pagrindinį vaidmenį pirimidino metabolizme. Pirimidinas suteikia pagrindinę struktūrą pirimidinų bazėms, citozinui, timinui ir uracilui, kurie atsiranda nukleorūgštyse. Tilaminas RNR keičiamas uracilu.
„Uracil“ taip pat gaminamas demitinuojant citidiną su citidino deaminaze. Cheminės pertvarkos tarp trijų pirimidino bazių yra nepaprastai svarbios DNR atstatymo procesams ir epigenetiniams pokyčiams. Epigenetikos kontekste įvairias savybes keičia aplinkos įtaka. Tačiau genetinė medžiaga nesikeičia. Organizmo modifikacijos pokyčius lemia skirtinga genų raiška. Kūno ląstelių diferenciacijos procesai formuojant skirtingas ląstelių linijas ir organus taip pat atspindi epigenetinį procesą, atsižvelgiant į ląstelės tipą, skirtingi genai yra įjungiami arba išjungiami.
Tai vyksta metilinant citidino bazes DNR. Metilinimo metu susidaro metilcitozinas, kurį deaminuojant galima paversti timinu. Komplementinis nukleobazės guaninas, esantis priešingoje dviguboje grandinėje, leidžia atpažinti klaidą ir vėl pakeisti timiną citozinu. Tačiau guaniną taip pat galima pakeisti adeninu, kuris lemia taškinę mutaciją. Jei nemetiliuotas citozinas yra deaminuotas, gaminamas uracilas. Kadangi uracilo DNR neatsiranda, jis iškart pakeičiamas citozinu. Vietoj citozino mutacijos dažnis dėl metilinimo šiek tiek padidėja.
Tuo pačiu metu vis daugiau ir daugiau genų išjungiami metilinant, kad ląstelės ląstelių linijoje taptų labiau specializuotos. Remonto procesuose taisymo fermentai yra pagrįsti originalia DNR grandine, kurią jie atpažįsta per didesnį metilinimo laipsnį. Papildoma kryptis taip pat sukurta remiantis joje saugoma informacija. Diegimo klaidos ištaisomos nedelsiant. Be to, fermentas PID (aktyvacijos sukelta citidino dezaminazė) labai specifiškai katalizuoja citidinų grupių dezaminavimą į uridino grupes viengrandėje DNR. Pasitaiko somatinių hipermutacijų, kurios keičia B ląstelių antikūnų sekas. Tada parenkamos atitinkančios B ląstelės. Tai įgalina lankstų imuninį atsaką.
Išsilavinimas, atsiradimas, savybės ir optimalios vertės
Citidinas yra tarpinis pirimidino metabolizmo produktas. Kaip atskiras ryšys, nesvarbu. Kaip jau minėta, jį sudaro citozino branduolio bazė ir svarainis cukraus ribozė. Kūnas pats gali sintetinti citoziną.
Tačiau jo sintezė yra labai daug energijos reikalaujanti, todėl ji yra atgaunama iš nukleorūgščių statybinių blokų pagal gelbėjimo kelią ir gali būti vėl integruota į nukleorūgštis. Kai bazė visiškai suskaidoma, susidaro anglies dioksidas, vanduo ir karbamidas. RNR jis yra kaip nukleozidas. DNR citozinas yra sujungtas su dezoksiriboze, todėl nukleozidų deoksicitidinas susidaro kaip statybinis blokas.
Ligos ir sutrikimai
DNR citidino liekanų metilinimas yra labai svarbus žymėjimui, norint atskirti įvairius biocheminius procesus. Tačiau metilinant gali atsirasti klaidų, dėl kurių atsiranda liga.
Esant netinkamam metilinimui, gali būti padidintas ir sumažėjęs genų aktyvumas, neatitinkantis reikalavimų. Šie metilinimo būdai perduodami dalijantis ląstelėms. Ilgainiui atsiranda pokyčių, kurie gali sukelti ligas. Pvz., Kai kurios naviko ląstelės turi skirtingas metilinimo struktūras, kurios neatsiranda sveikose ląstelėse. Pavyzdžiui, metilinimas gali blokuoti tam tikrus genus, kurie koduoja augimą reguliuojančius fermentus. Jei šių fermentų trūksta, gali atsirasti nekliudomas ląstelių augimas. Tai taip pat taikoma fermentams, kurie inicijuoja tvarkingą ląstelių mirtį (apoptozę), kai atsiranda ląstelių defektų.
Tikslinė įtakos DNR metilinimui dar nėra įmanoma. Tačiau yra tyrimų, susijusių su visišku naviko ląstelių demetilinimu, siekiant vėl kontroliuoti augimą reguliuojančius baltymus. Remiantis keliais klinikiniais tyrimais, nustatyta, kad demetilinimas riboja naviko augimą pacientams, sergantiems ūmine mieloidine leukemija. Ši procedūra dar vadinama epigenetine terapija. Metilinimo procesai taip pat gali turėti įtakos kitoms ligoms. Dėl aplinkos įtakos organizmas prisitaiko prie pasikeitusių sąlygų, susidaręs biologinis modifikavimas, pagrįstas DND citidino liekanų metilinimu. Taigi kūnas vykdo mokymosi procesą, kuris taip pat gali sukelti neteisingą reguliavimą.







.jpg)













.jpg)